暔幙偺嶰懺偲擬塣摦乮俀乯 |
|
掅壏乮0 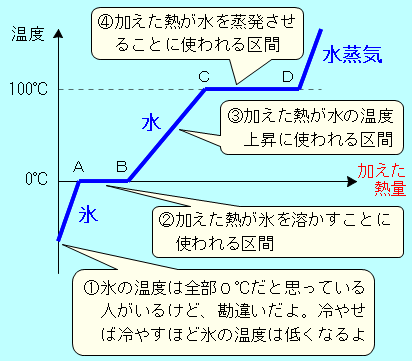 俙揰偱0 俙俛娫偼丄擬傪壛偊懕偗偰偄傞偺偵壏搙偑忋偑傜側偄偺偼丄壛偊偨擬乮僄僱儖僊乕乯偑屌懱偺悈暘巕偳偆偟偺寢崌傪愗抐偡傞偨傔偵巊傢傟偰偄傞偐傜偱偡丅屌懱傪塼懱偵偡傞偨傔偵昁梫側擬検傪梈夝擬偲偄偄傑偡丅 俠俢娫傕丄擬傪壛偊懕偗偰偄傞偺偵壏搙偑忋偑傜側偄偺偼丄壛偊偨擬乮僄僱儖僊乕乯偑塼懱偺悈暘巕偳偆偟偺寢崌傪愗抐偡傞偨傔偵巊傢傟偰偄傞偐傜偱偡丅塼懱傪婥懱偵偡傞偨傔偵昁梫側擬検傪忲敪擬偲偄偄傑偡丅 摨偠0 傑偨丄摨偠100 偙偺偙偲偐傜丄梈夝擬傗忲敪擬偺傛偆偵丄忬懺傪曄壔偝偣傞偨傔偵巊傢傟傞擬傪愽擬偲偄偄傑偡丅乮愽悈娡偺愽偩傛乯 梈夝擬傗忲敪擬偼丄1倗偁偨傝偳傟偔傜偄偺擬検偑昁梫偐偱昞偝傟傞偺偱丄扨埵偼丄俰/倗乮僕儏乕儖枅僌儔儉乯偲側傝傑偡 丅
|
||||||||
| 丂 | ||||||||
| 丂仺 栤戣 傊丂 |
||||||||
| |
||||||||